Содержание
| Гидропероксильный радикал | |
|---|---|
 ( <<<картинка>>> ) |
|
| Общие | |
| Систематическое наименование |
Гидропероксил |
| Традиционные названия | гидродиоксид гидродиоксил |
| Хим. формула | HO2 |
| Физические свойства | |
| Молярная масса | 33,01 г/моль |
| Химические свойства | |
Константа диссоциации кислоты p K a <displaystyle pK_>  |
4.88 [1] |
| Классификация | |
| Рег. номер CAS | 3170-83-0 |
| PubChem | 520535 |
| SMILES | |
| ChEBI | 25935 |
| ChemSpider | 454055 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гидропероксильный радикал или пероксильный радикал — это протонированная форма супероксида с формулой HO2•.
Содержание
Образование [ править | править код ]
Гидропероксильный радикал образуется в результате переноса атома водорода на молекулу кислорода, путём взаимодействия атома кислорода с гидроксильным радикалом (HO•) или протона с супероксид анионом [2] .
Химические свойства [ править | править код ]
В водном растворе супероксид анинон O2 − и гидропероксильный радикал находятся в равновесии:
O2 − + H2O  HO2 + OH −
HO2 + OH −
Константа равновесия этого процесса pKa = 4.88 [3] , из чего можно сделать вывод, что 0,3 % супероксида в цитозоле находится в протонированной форме.
В отличие от O2 − , который является сильным восстановителем, HO2• в ходе многих биологически важных реакций может вести себя как окислитель, отбирая атомы водорода от токоферола и полиненасышенных жирных кислот липидной мембраны. По этой причине он является одним из основных инициаторов перекисного окисления липидов.
Поскольку диэлектрическая постоянная сильно влияет на pKa, а диэлектрическая проницаемость воздуха весьма мала, образующийся (фотохимически) в атмосфере супероксид практически полностью существует в форме HO2•. Поскольку HO2• весьма реакционноспособен, он действует как атмосферное «моющее средство», разлагая некоторые органические загрязнители. По этой причине химия HO2 имеет геохимическое значение.
Воздействие на окружающую среду [ править | править код ]
Гидропероксильный радикал разрушает озоновый слой стратосферы; он образуется в результате окисления углеводородов в тропосфере [2] .
Гидропероксильный радикал или пероксильный радикал — это протонированная форма супероксида с формулой HO2•.
| Гидропероксильный радикал | |
|---|---|
 ( <<<картинка>>> ) |
|
| Общие | |
| Систематическое наименование |
Гидропероксил |
| Традиционные названия | гидродиоксид гидродиоксил |
| Хим. формула | HO2 |
| Физические свойства | |
| Молярная масса | 33,01 г/моль |
| Химические свойства | |
Константа диссоциации кислоты p K a <displaystyle pK_>  |
4.88 [1] |
| Классификация | |
| Рег. номер CAS | 3170-83-0 |
| PubChem | 520535 |
| SMILES | |
Содержание
Гидропероксильный радикал образуется в результате переноса атома водорода на молекулу кислорода, путём взаимодействия атома кислорода с гидроксильным радикалом (HO•) или протона с супероксид анионом [2] .
В водном растворе супероксид анинон O2 − и гидропероксильный радикал находятся в равновесии:
Константа равновесия этого процесса pKa = 4.88 [3] , из чего можно сделать вывод, что 0,3 % супероксида в цитозоле находится в протонированной форме.
В отличие от O2 − , который является сильным восстановителем, HO2• в ходе многих биологически важных реакций может вести себя как окислитель, отбирая атомы водорода от токоферола и полиненасышенных жирных кислот липидной мембраны. По этой причине он является одним из основных инициаторов перекисного окисления липидов.
Поскольку диэлектрическая постоянная сильно влияет на pKa, а диэлектрическая проницаемость воздуха весьма мала, образующийся (фотохимически) в атмосфере супероксид практически полностью существует в форме HO2•. Поскольку HO2• весьма реакционноспособен, он действует как атмосферное «моющее средство», разлагая некоторые органические загрязнители. По этой причине химия HO2 имеет геохимическое значение.
Гидропероксильный радикал разрушает озоновый слой стратосферы; он образуется в результате окисления углеводородов в тропосфере [2] .

 |
|
 |
|
| Names | |
|---|---|
| Preferred IUPAC name | |
| Other names | |
| Identifiers | |
|
|
| Properties | |
| H O 2 | |
| Molar mass | 33.006 g·mol −1 |
| Acidity (pKa) | 4.88 [1] |
| Basicity (pKb) | 9.12 (basicity of superoxide ion) |
| Conjugate base | Superoxide anion |
|
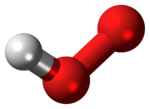
The hydroperoxyl radical, also known as the perhydroxyl radical, is the protonated form of superox >[2] ContentsStructure and reactions [ edit ]The molecule has a bent structure. [3] The superox >O − The pKa of HO2 is 4.88. Therefore, about 0.3% of any superox >[4] Reactive oxygen species in biology [ edit ]Importance for atmospheric chemistry [ edit ]Gaseous hydroperoxyl is involved in reaction cycles that destroy stratospheric ozone. It is also present in the troposphere, where it is essentially a byproduct of the ox >[5] Because dielectric constant has a strong effect on pKa, and the dielectric constant of air is quite low, superoxide produced (photochemically) in the atmosphere is almost exclusively present as HO2. As HO2 is quite reactive, it acts as a "cleanser" of the atmosphere by degrading certain organic pollutants. As such, the chemistry of HO2 is of considerable geochemical importance. |
|

 Y
Y